Artículos originales
Intervalo de referencia para la cistatina C en una muestra de población adulta cubana
Reference Interval for Cystatin C in a Sample of Adult Cuban Population
Cómo citar este artículo:
Copyright: Esta revista provee acceso libre inmediato a su contenido bajo el principio de que hacer disponible gratuitamente investigación al publico apoya a un mayor intercambio de conocimiento global. Esto significa que se permite la copia y distribución de sus contenidos científicos por cualquier medio siempre que mantenga el reconocimiento de sus autores, no haga uso comercial de las obras y no se realicen modificaciones de ellas.

Recibido: 2019-02-26 10:13:02
Aprobado: 2020-04-01 16:13:44
Correspondencia: Dailen Darias Rivera. Complejo Científico Ortopédico Internacional Frank País. La Habana. dailendarias@infomed.sld.cu
RESUMEN
Objetivo: establecer el intervalo de referencia de la cistatina C en una muestra de la población adulta cubana, en el laboratorio del Hospital Clínico Quirúrgico Hermanos Ameijeiras.
Método: estudio descriptivo de corte transversal en 249 donantes de sangre (hombres y mujeres en igual proporción), con edades comprendidas entre 18 y 50 años. Se obtuvieron por método inmunoturbidimétrico los valores séricos de cistatina C y se compararon por sexo y grupo etáreo. Se calculó el intervalo de referencia y se comparó con el propuesto por el fabricante.
Resultados: el intervalo de referencia obtenido mostró asociación con el sexo, pero no con el grupo etáreo. Se encontraron diferencias estadísticamente significativas entre el intervalo de referencia sérico de cistatina C en ambos sexos y el propuesto por el fabricante.
Conclusiones: el intervalo de referencia obtenido en esta investigación para cada sexo fue más alto que lo planteado por el fabricante del reactivo utilizado, ambos límites del intervalo tuvieron valores más elevados, se encontró además diferencia estadísticamente significativa entre ambos. Se evidenció la necesidad de disponer en cada laboratorio clínico, de valores de referencia acordes a cada lugar, según recomiendan las instituciones internacionales.
Palabras clave: cistatina C; valores de referencia; adulto
ABSTRACT
Objective: to establish the interval of reference of Cystatin C in a sample of adult Cuban population, in the laboratory of the Clinical Surgical Hospital Hermanos Ameijeiras.
Method: cross-descriptive study in 249 blood donors (women and men in the same proportion), aged between 18 and 50. By the inmunoturbidimetric method the values of seric cystatin C were obtained and were compared by sex and age group. The interval of reference was calculated and compared with the one proposed by the manufacturer.
Results: the interval of reference obtained showed association with sex, but not with the age group. Statistically significant differences were found between the interval of seric reference of cystatin C in both sexes and the one proposed by the manufacturer.
Conclusion: the need of counting with values of reference according to each place was evidenced, according to the International Federation of Clinical Chemistry and the standards of clinical laboratory.
Key words: cystatin C; reference values; adult
INTRODUCCIÓN
La cistatina C es una proteína de baja masa molar cuyo estudio ha despertado un interés creciente desde el año 1985 cuando Simonsen y cols. demostraron que su concentración en suero presentaba una correlación negativa con la tasa de filtrado glomerular.(1)
Constituye una herramienta diagnóstica superior a la creatinina en la detección de una alteración precoz de la función renal. Añade información de interés en pacientes con valores de filtrado glomerular entre 20 y 60 mL/min/1,73m2 donde el uso de la ecuación del estudio Modificación de la Dieta en Enfermedad Renal es inadecuado (individuos con alteraciones en la masa muscular, síndrome nefrótico, insuficiencia hepática y enfermedad renal crónica agudizada). Además, parece aportar información útil en individuos de edad avanzada, pacientes diabéticos, hipertensos y con enfermedades oncológicas. La cistatina C ha demostrado su superioridad sobre las ecuaciones basadas en la creatinina en pacientes con pesos extremos (en anorexia y obesidad), en pacientes con miembros amputados y en pacientes con enfermedades neuromusculares y en el embarazo.(2)
La concentración sérica de cistatina C no se afecta significativamente por los cambios en la masa muscular, lo cual es una ventaja frente a la creatinina en la valoración de la función renal en la población en edad pediátrica.(3,4)
Estudios recientes sugieren que aumentos de la concentración de cistatina C pueden también indicar mayor riesgo de enfermedad cardiovascular y fallo cardíaco, accidente vascular cerebral y puede asociarse incluso a mayor mortalidad.(5)
La determinación de los rangos de referencia para los análisis químicos realizados en un laboratorio, constituye requisito imprescindible a la hora de implementar un programa de control de calidad adecuado.(6)
Cada laboratorio usa diferentes tipos de instrumentación y diferentes métodos de análisis. Esto implica que los laboratorios deben establecer sus propios valores de referencia. Por tanto, el paciente y el médico deben utilizar el valor de referencia proporcionado por el laboratorio que realiza el análisis en lugar de valores teóricos o ideales u obtenidos de algún libro.(7)
La Federación Internacional de Química Clínica y el Instituto de Estándares de Laboratorio Clínico han elaborado recomendaciones para la producción de valores de referencia biológicos poblacionales.(8,9)
En el laboratorio del Hospital Clínico Quirúrgico Hermanos Ameijeiras no se ha validado la cistatina C para su uso y no se encontró literatura publicada sobre el tema en población adulta cubana. La importancia de las aplicaciones clínicas de este analito y las recomendaciones por parte de estas instituciones para el trabajo de los laboratorios clínicos, fundamentan la realización del presente estudio. La identificación oportuna de alteraciones en la función renal, cardiovascular y neurológica, es necesaria para lograr la instauración oportuna del tratamiento, que garantice beneficios tanto clínicos como económicos a los pacientes. Con el resultado alcanzado se podrá obtener un diagnóstico más certero y confiable en las diferentes patologías clínicas implicadas e imponer un tratamiento precoz que les permita una mejor calidad de vida y menos complicaciones.
Fue objetivo de este estudio establecer el intervalo de referencia de la cistatina C en una muestra de la población adulta cubana, en el laboratorio del Hospital Clínico Quirúrgico Hermanos Ameijeiras.
MÉTODOS
Se realizó un estudio descriptivo de corte transversal, para identificar el intervalo de referencia de la cistatina C en una muestra de la población adulta cubana, en el laboratorio clínico del Hospital Clínico Quirúrgico Hermanos Ameijeiras de La Habana.
El universo estuvo conformado por todos los adultos sanos que acudieron a realizar donación de sangre al banco de sangre del Hospital Clínico Quirúrgico Hermanos Ameijeiras y del Hospital Militar Central Dr. Carlos Juan Finlay durante el año 2016, tiempo en que se realizó la investigación.
Se consideraron los siguientes criterios de selección: adultos supuestamente sanos con edad comprendida entre 18 y 50 años, haber cumplido con los criterios del banco de sangre para ser donante, no tener un embarazo, sin hábito de fumar, ni ingestión de bebidas alcohólicas, normopeso, ausencia de enfermedad renal crónica, trastorno tiroideo u otra enfermedad crónica no transmisible, que no hubiera ingerido medicamentos.
Se excluyeron a los sujetos supuestamente sanos que no aceptaron participar en el estudio, resultados con valores aberrantes (entendiéndose estos como aquellos valores de referencia que se encuentran alejados del conjunto constituido por el resto de la muestra de referencia), sujetos con estudio previo de creatinina por encima de parámetros de referencia.
Se estudiaron todos los pacientes que cumplieron con los criterios de selección antes señalados. La población de estudio fue seleccionada de forma intencional, acorde a lo planteado por la Federación Internacional de Química Clínica y el Instituto de Estándares de Laboratorio Clínico,(6-9) por lo que quedó conformada finalmente por 249 sujetos, 125 hombres y 124 mujeres.
Para cumplir los objetivos propuestos se operacionalizaron las siguientes variables:
- Edad
Se consideró en años cumplidos. Se clasificó en 4 grupos prediseñados.
Escala de clasificación:
< 20 años
20- 29 años
30- 39 años
40– 50 años
- Sexo
Es el sexo del paciente según el genotipo del paciente.
Escala de clasificación:
Femenino
Masculino
- Cistatina C
Variable obtenida en el laboratorio. Se informó en unidades de mg/L.
Valores de referencia del fabricante: 0,59 – 1,03 mg/L
Se llevó a cabo una búsqueda en diversas fuentes, se revisaron revistas impresas actualizadas sobre el tema y trabajos digitales en revistas de impacto científico.
La fuente del dato primario se obtuvo a partir de la hoja de recolección de datos. Todas las personas fueron informadas acerca de las características y el objetivo del estudio para obtener de ellas el consentimiento.
Los parámetros a recoger fueron: nombre y apellidos, edad, sexo, peso, talla, índice de masa corporal, tensión arterial, antecedentes patológicos personales, hábitos tóxicos, ingestión de medicamentos. Todos ellos se registraron en computadora en una base de datos en Excel, donde también se almacenaron los resultados obtenidos en las determinaciones.
Todos los sujetos sanos entrevistados fueron examinados físicamente. A los que fueron aceptados finalmente como donantes, se les realizó la extracción de sangre venosa, en ayunas, en la región cubital para las determinaciones a realizar, siguiendo los procedimientos establecidos por las buenas prácticas y bioseguridad de laboratorio clínico.
La muestra de sangre fue depositada en tubo de 12 x 75 mm, sin anticoagulante, centrifugada después de retraído el coágulo y conservado el suero en congelación a –20oC cuando no fue utilizado en fresco, hasta un período máximo de 2 meses.
Fueron procesadas en el equipo automatizado Inlab 240 de la firma italiana CPM que se encuentra en el departamento de ensayos clínicos del laboratorio del Hospital Clínico Quirúrgico Hermanos Ameijeiras con el objetivo de garantizar la trazabilidad del estudio.
Se determinó la creatinina y si los valores se encontraban dentro del intervalo de referencia, se realizó la determinación de la cistatina C. Ambas determinaciones utilizaron el reactivo brindado por la firma CPM.
Determinación de la concentración sérica de creatinina
Esta determinación solo se realizó con el objetivo de incluir o excluir pacientes de la muestra. Se realizó por el método enzimático colorimétrico PAP, con reactivos de la firma italiana CPM.
Valores de referencia para el método utilizado:
Hombres: 79 – 115 µmol/L.
Mujeres: 53 – 97 µmol/L.
Determinación de la concentración sérica de cistatina C
Se utilizó reactivo de la firma italiana CPM. Se realizó por método inmunoturbidimétrico, basado en la reacción que ocurre entre la cistatina C y las partículas de látex recubiertas con anticuerpos específicos contra cistatina C humana, lo que produce una reacción de aglutinación que genera un cambio en la absorbancia proporcional a la cantidad de cistatina C en la muestra. Los valores en este método son determinados utilizando mediciones de punto final con corrección del reactivo blanco. La relación entre la absorbancia y la concentración permite un sistema multipunto con un rango de medida entre 0,05 y 10 mg/L. La temperatura de medición es a 37 oC. Se leyó a una longitud de onda de 550nm.
Para el control de calidad se utilizaron los controles de cistatina C CPM bajo y alto que ofrece el fabricante con los siguientes rangos de concentraciones:
Control bajo: 0,8- 1,2 mg/L.
Control alto: 3,04- 4,56 mg/L.
Valores de referencia del fabricante descritos anteriormente.
Precisión del método Intraensayo
CV (%) 0,70 1,22 1,54 3,37
Luego de obtenidos los valores séricos de cistatina C, fue analizada su variabilidad en cada sexo y grupo de edad, para finalmente calcular el intervalo de referencia.
El procesamiento de los datos se realizó utilizando una base de datos en Excel y el empleo de los programas estadísticos SPSS versión 20,0 y EPIDAT versión 3,0. Para cumplimentar los objetivos propuestos, se analizaron las variables seleccionadas mediante el cálculo de números absolutos y porcentajes (%) como medidas de resumen para variables cualitativas. Para las variables cuantitativas se consideraron medidas de tendencia central y dispersión para evaluar la distribución de los datos, y se realizaron histogramas de frecuencias.
Se corroboró el cumplimiento del supuesto de normalidad para los valores de cistatina C según sexo y grupo etáreo, a través del estadístico de Kolmogorov-Smirnov con corrección de la significación de Lilliefors. Se identificaron los valores aberrantes por el método gráfico (diagrama de cajas) y fueron eliminados.
Como método de análisis para evaluar la asociación entre variables cuantitativas se empleó el ANOVA de un factor, lo que permitió comparar los resultados según sexo y grupo etáreo. Se calculó el intervalo de referencia a distancia de ± 2 desviaciones estándar (σ) de la media. Para evaluar el contraste sobre una media para valores de cistatina C y comparar el intervalo obtenido con el del fabricante, se utilizó la Prueba para una media (Estadístico t).
En todas las pruebas estadísticas realizadas se utilizó un nivel de significación de 0,05 y una confiabilidad del 95 %. Las diferencias fueron consideradas estadísticamente significativas cuando el valor de p fue menor que 0,05.
Los resultados se presentan en forma tabular y gráfica, utilizando para su tabulación, cálculos de indicadores, tratamiento del texto y demás componentes del informe final, el paquete Office 2016 (Word y Excel), con ambiente de Windows 10.
Antes de su inclusión en el estudio, cada paciente recibió una explicación de la investigación y su finalidad. Se tomó por escrito el consentimiento informado del paciente sobre su libre participación en el estudio. Se tuvieron en cuenta los principios básicos de la ética, de respeto, dando autonomía a las personas, haciendo uso de la beneficencia en el manejo y divulgación de los datos y sobre todo aplicando la justicia en la investigación.
RESULTADOS
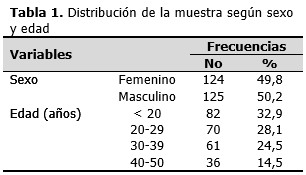
En total participaron 249 sujetos, distribuidos en 124 mujeres y 125 hombres, para un 49,8 % y 50,2 % respectivamente del total de la muestra. La edad promedio de todos los participantes del estudio fue de 28 años, con un rango entre 18 y 50. El grupo de menores de 20 estuvo conformado por 82 sujetos para un 32,8 % del total, el mayor en el estudio, seguido por los de 20 - 29 años y los de 30 – 39 años que fueron el 28 % y el 24% respectivamente. (Tabla 1).
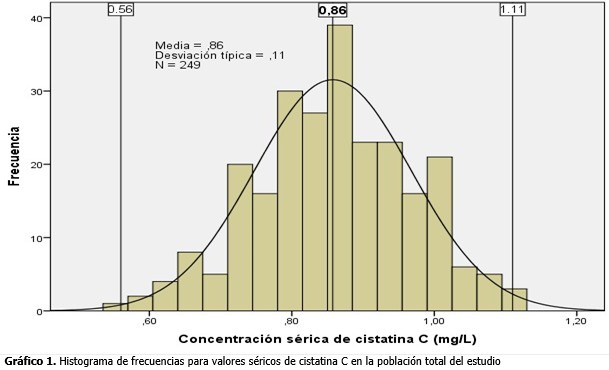
Cuando se analizaron los valores séricos de cistatina C en el estudio, se obtuvo una media de 0,857 mg/L. con un intervalo de confianza del 95 % para la media entre 0,845 y 0,875, y una desviación estándar (σ) de 0,11. Al analizar la prueba de normalidad de Kolmogorov-Smirnov con corrección de la significación de Lilliefors, se observó que el valor del estadístico (p = 0,20) se encontraba por encima del valor de significación estadística (0,05), por lo que se concluyó que la variable cistatina C tiene una distribución normal. Se muestra a continuación el histograma de frecuencias para todos los valores de cistatina C obtenidos en el estudio (n= 249). El rango de valores estuvo entre 0,56 y 1,11 mg/L (mostrados ambos por dos líneas perpendiculares al eje de las abscisas). Se superpone la curva de normalidad y se observa la distribución normal de la variable. Se muestran además los valores de la media y la desviación estándar calculados. (Gráfico 1).
La variable cistatina C tuvo una distribución normal en ambos sexos según la prueba de normalidad calculada. Se presentan los valores de la media, desviación estándar y el intervalo de confianza para la media del 95 %. Se encontró que el valor de la media en los hombres (0,875 mg/L) fue mayor que en las mujeres (0,839 mg/L), y al analizar la asociación entre ambas se encontró diferencia estadísticamente significativa (p = 0,011). En el sexo masculino los resultados tuvieron un rango de valores más amplio (0,56 – 1,11 mg/L) con respecto a las mujeres (0,62 - 1,10 mg/L). (Tabla 2).
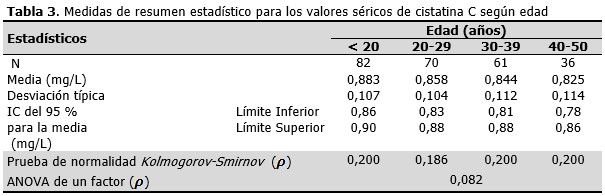
Posteriormente se analizó la variabilidad de la cistatina C según los grupos de edades. Para cada uno de los grupos se presentan medidas de resumen de los resultados obtenidos y se analizó si estos valores variaban de acuerdo a la edad. (Tabla 3).
Se analizó la distribución de los valores al realizar la prueba de normalidad de Kolmogorov-Smirnov con corrección de la significación de Lilliefors. Los valores de p se encontraron por encima de 0,05 en todos los casos, por lo que se planteó que la cistatina C se distribuye de manera normal en cada grupo etáreo estudiado. Se calculó la media y el intervalo de confianza del 95 % para la media en cada grupo, no se encontraron diferencias estadísticamente significativas entre ellos (valor de p = 0,082). Se contrastó el valor de la media de cistatina C obtenido en el estudio con los valores según sexo y grupos de edades. (Tabla 4).
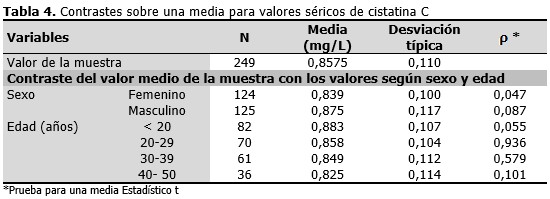
Al analizar el contraste sobre una media entre los valores de cistatina C del estudio y los valores para cada sexo, se encontró que sí hubo diferencias estadísticamente significativas con el sexo femenino (p < 0,05), mientras que con el sexo masculino no las hubo. Igualmente se contrastaron los valores de la media de la cistatina C con los valores obtenidos para cada grupo de edad. En cada caso el valor de p estuvo por encima de 0,05, por lo que no se encontró asociación estadística entre ambas variables.
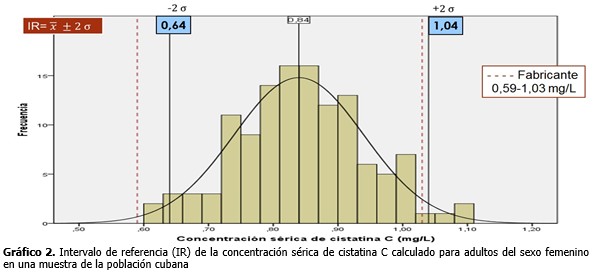
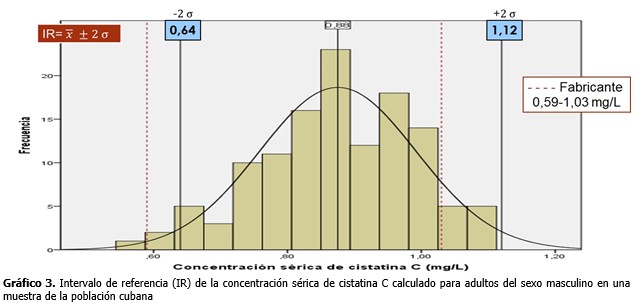
Como previamente se comprobó que existía asociación estadística de la cistatina C con el sexo, específicamente con el sexo femenino, se calculó entonces un intervalo de referencia para cada sexo, para una mejor interpretación de los resultados. Como además se demostró que la variable tenía una distribución normal, el intervalo fue calculado a la distancia de ±2 σ de la media. Se observó además que el intervalo de referencia para los hombres fue más elevado que para las mujeres, ya que en este grupo se obtuvo un valor más alto de la media y mayor desviación estándar. (Gráficos 2 y 3).
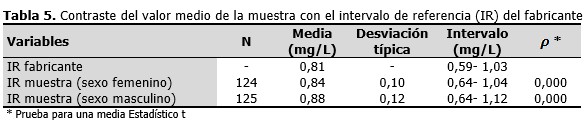
Se muestra el resultado del contraste para una media, realizado entre el intervalo de referencia obtenido en el estudio para cada sexo y el intervalo brindado por el fabricante. Se encontró que sí hubo diferencias estadísticamente significativas entre ambos intervalos biológicos de referencia, siendo el valor de la media del estudio en cada caso, mayor que la media del fabricante. Se evidenció un aumento en los valores de ambos límites del intervalo con respecto al del fabricante. (Tabla 5).
DISCUSIÓN
La identificación de los valores de referencia en cada población es responsabilidad del laboratorio clínico local mediante el procedimiento recomendado por la Federación Internacional de Química Clínica, esto permite homogeneizar los criterios para la obtención de intervalos de referencia en los distintos países y facilita el análisis de la variabilidad biológica entre las diferentes razas. Por lo anterior, los valores conocidos tradicionalmente como normales están sujetos indudablemente a la variabilidad biológica individual y colectiva, debido a ello es necesario incluir los factores de variabilidad dentro de su definición. Por consecuencia, es necesario determinar la magnitud de los valores en cada población, así como en la partición de esta (género, edad, etcétera).(10,11)
Pero la realidad es otra, y en este caso, las recomendaciones se han seguido muy poco, probablemente debido a las dificultades económicas y prácticas que conlleva la producción de valores de referencia.
Las normas plantean que los intervalos de referencia biológicos se deben revisar periódicamente. Si el laboratorio tiene razones para creer que un intervalo particular ya no es apropiado para la población de referencia, entonces se debe iniciar una investigación, seguida si es necesario, de la correspondiente acción correctiva.(11)
Sobre el análisis del intervalo biológico de la cistatina C en adultos sanos, se encontró muy poco en la literatura reciente. Solamente se encontraron trabajos relacionados en edades pediátricas.(3,4,12) La mayor parte de la bibliografía encontrada sobre valores de cistatina C en población sana data de 10 años o más.
Varios trabajos revisados tratan la relación de esta variable con el sexo y la edad. La mayoría de los estudios demuestra la existencia de una muy ligera diferencia en las concentraciones de cistatina C entre sexos, lo que no justifica la necesidad de disponer de rangos distintos de concentración por género.(2,13) La compañía Biosystems SA en el año 2015 realizó el lanzamiento del reactivo de la cistatina C, e igualmente plantearon la constancia de los valores independiente de la edad o sexo.(14)
Otras expresan diferencias entre ambos sexos, siendo los valores ligeramente superiores en los hombres, tal y como se encontró en este estudio.(10) En una revisión publicada en los Anales de Pediatría en el año 2012, aparecen valores diferentes en el intervalo de referencia para hombres y mujeres, con valores un poco más elevados en los hombres, al igual que en otro estudio publicado en el 2001 en la revista de Laboratorio Médico y Química Clínica.(15,16)
A pesar de esto, los diferentes fabricantes de reactivos no especifican valores para cada sexo en sus insertos, incluyendo los de la firma CPM empleados en esta investigación.(5,17-20)
En cuanto a la edad, se plantea que los valores de cistatina C son mayores en edades pediátricas y aumentan nuevamente después de los 50 años, debido al deterioro propio de la función renal en el adulto mayor. Sin embargo, en las edades comprendidas entre 18 y 50 años, no existe variación significativa, por lo que puede adoptarse un valor único para estas etapas de la vida. Pequeñas variaciones en los intervalos de referencia publicados pueden deberse a diferencias atribuibles al calibrador empleado con los diferentes métodos de determinación. Se revisaron varias publicaciones internacionales, incluso de fabricantes y todos coinciden en este punto.(3,4,12,14-16)
Esta conclusión concuerda con los resultados de este estudio, ya que, como se demostró en los resultados, no hubo tampoco diferencias que fueran de significación estadística entre los distintos grupos de edades estudiados, así como tampoco entre el valor medio para el total de sujetos y el valor medio para las diferentes edades.
Pequeñas variaciones en los intervalos de referencia publicados pueden deberse a diferencias atribuibles al calibrador empleado con los diferentes métodos de determinación. La mayoría de los autores que proveen datos sobre valores de referencia, como se ha comentado anteriormente, concluyen que, entre los 12 meses y los 50 años, la concentración de cistatina C es independiente de la edad, el sexo, la talla y el peso.
Son muy pocos los laboratorios clínicos en el mundo que siguen las recomendaciones de la Federación Internacional de Química Clínica y de la Sociedad Europea de Química Clínica. Esto se debe a las dificultades en la consecución de individuos de referencia y al coste económico. En la realidad, los laboratorios clínicos siguen diversas opciones con diferente rigor científico.(20)
Muchos laboratorios clínicos utilizan los intervalos de referencia del analito incluidos en los insertos del reactivo comercial para reportar los resultados, sin embargo, los intervalos de referencia para cistatina C notificados en la literatura son muy variados, siendo esta variación el resultado de la utilización de diferentes métodos para calcular estos intervalos, así como las diferentes características de las poblaciones utilizadas en dichos estudios.(8,9,20)
Los valores de referencia que proveen los diferentes fabricantes de reactivos también difieren entre sí.(5,14,17-20)
El intervalo de referencia obtenido en esta investigación para cada sexo fue más alto que lo planteado por el fabricante del reactivo utilizado, es decir, ambos límites del intervalo tuvieron valores más elevados, se encontró además diferencia estadísticamente significativa entre ambos. Estos resultados apoyan aún más la idea de que cada laboratorio debe establecer sus propios valores de referencia, ya que las características de cada población son diferentes, así como las características técnicas de los equipos que se utilizan. En lo adelante, se sugiere, que para estudios en la población cubana se pudieran utilizar los resultados de esta investigación. No obstante, sería conveniente, a pesar de que en la población que asiste al Hospital Hermanos Ameijeiras existe una amplia representación de habitantes del país, que se realicen estudios similares en otros laboratorios.
Conflicto de intereses: la autora declara la no existencia de conflictos de intereses relacionados con el estudio.
Contribución de los autores:
La autora expone que la idea conceptual, el análisis estadístico, la revisión de la literatura y la escritura del artículo corresponden a su autoría.
Financiación: Complejo Científico Ortopédico Internacional Frank País. La Habana.REFERENCIAS BIBLIOGRÁFICAS
- Simonsen O, Grubb A, Thysell H. The blood serum concentration of cystatin C (gamma-trace) as a measure of the glomerular filtration rate. Scand J Clin Lab Invest. 1985;45(2):97-101 [Buscar en Google Scholar]
- Martínez C. Cistatina C. Propiedades y utilidad clínica. Ed Cont Lab Clín. 2006;9(2):36-41 [Buscar en Google Scholar]
- Cabrera M. Cistatina C versus creatinina como marcador del filtrado glomerular en prematuros de muy bajo peso, evolución de cero a dos años de edad [Internet]. Madrid: Universidad Autónoma de Madrid; 2013 [citado 26 May 2019]. Disponible en: https://dialnet.unirioja.es/servlet/tesis?codigo=39356 [Buscar en Google Scholar]
- Fraga GM, Huertes B. Evaluación básica de la función renal en Pediatría. Protoc diagn ter pediatr. 2014;1(1):21-35 [Buscar en Google Scholar]
- American Association for Clinical Chemistry. Cistatina C [Internet]. Washington D.C: AACC; 2015 [citado 24 Mar 2019]. Disponible en: http://www.labtestsonline.es/tests/CystatinC.html?tab=2 [Buscar en Google Scholar]
- Fuentes X. Intervalos de referencia biológicos. NOTICONAQUIC [revista en Internet]. 2011 [citado 19 Oct 2018];54(1):[aprox. 6p]. Disponible en: http://www.ifcc.org/media/215857/Intervalos de referencia biológicos DIV.pdf [Buscar en Google Scholar]
- American Association for Clinical Chemistry. Intervalos de referencia y su significado [Internet]. Washington D.C: AACC; 2015 [citado 20 May 2019]. Disponible en: http://www.labtestsonline.es/tests/Intervalosdereferencia.html?tab=2 [Buscar en Google Scholar]
- Westgard JO. Validación básica del método. Entrenamiento en Gestión de la Calidad Analítica para Laboratorios Clínicos. Madison: Edición Wallace Coulter; 2013 [Buscar en Google Scholar]
- International Federation of Clinical Chemistry and Laboratory. Medicine Statement on the use of ISO 15189 in the accreditation of medical laboratories [Internet]. Milán: IFCCL; 2015 [citado 12 Oct 2019]. Disponible en: http://www.ifcc.org/pdf/iso15189_c-clm.pdf [Buscar en Google Scholar]
- Olay G, Díaz P, Hernández R, Cervantes RD, Presno JM, Alcántara LE. Determinación de intervalos de referencia para química clínica en población mexicana. Rev Latinoamer Patol Clin. 2013;60(1):43-51 [Buscar en Google Scholar]
- Fuentes X. Valores de referencia biológicos, acreditación y armonización. Laboratorio Clínico. 2012;5(1):55-6 [Buscar en Google Scholar]
- Salazar M, Parra I, Klunder M, Martínez M. Cistatina C como prueba de rutina para evaluar la función renal en pacientes pediátricos. Acta bioquím clín latinoam [revista en Internet]. 2015 [citado 28 Sep 2019];49(2):[aprox. 10p]. Disponible en: https://www.researchgate.net/publication/282764001_Cistatina_C_como_prueba_de_rutina_para_evaluar_la_funcion_renal_en_pacientes_pediatricos [Buscar en Google Scholar]
- Hospital Italiano de Buenos Aires. Dosaje de Cistatina C - Marcador más sensible y precoz que la creatinina [Internet]. Buenos Aires: HIBA; 2016 [citado 20 Dic 2019]. Disponible en: https://www.hospitalitaliano.org.ar/#!/home/comercial/noticia/9201 [Buscar en Google Scholar]
- Biosystem SA. Lanzamiento de cistatina C [Internet]. Madrid: Universidad Complutense de Madrid; 2015 [citado 28 Ene 2016]. Disponible en: http://www.biosystems.pt/news/ES000192 [Buscar en Google Scholar]
- Fraga G. La determinación de los valores plasmáticos de cistatina C como método de valoración de la función renal en pediatría. An Pediatr Contin. 2012;10(2):95-100 [Buscar en Google Scholar]
- Galteau M, Guyon M, Gueguen R, Siest G. Determination of serum cystatin C: Biological variation and reference values. Clin Chem Lab Med. 2001;39(9):850-7 [Buscar en Google Scholar]
- Benavides A, Rodríguez Y, González D, Martínez I, Hernández I, Vilaboy B. Utilización del biomarcador de cistatina C en pacientes con posible fallo renal. Finlay [revista en Internet]. 2019 [citado 13 Ene 2020];9(4):[aprox. 7p]. Disponible en: http://revfinlay.sld.cu/index.php/finlay/article/view/717 [Buscar en Google Scholar]
- Wiener Lab. Método inmunoturbidimétrico para la determinación de cistatina C [Internet]. Rosario. Argentina: Wiener Laboratorios; 2000 [citado 20 Jun 2019]. Disponible en: http://www.wiener-lab.com.ar [Buscar en Google Scholar]
- Mite MA. La Cistatina C como indicador de función renal y valoración de tasa de filtración glomerular [Internet]. Manabí: Unversidad Estatal del Sur de Manabí; 2010 [citado 18 Abr 2019]. Disponible en: http://repositorio.unesum.edu.ec/bitstream/53000/531/1/Lab-Cli-2010-04.pdf [Buscar en Google Scholar]
- Fuentes X. La normalización en ciencias de laboratorio clínico. Rev Lab Clin [revista en Internet]. 2016 [citado 27 May 2019];9(3):[aprox. 12p]. Disponible en: https://www.elsevier.es/es-revista-revista-del-laboratorio-clinico-282-articulo-la-normalizacion-ciencias-laboratorio-clinico-S1888400816300277 [Buscar en Google Scholar]
Enlaces refback
- No hay ningún enlace refback.
FINLAY EN: 








FINLAY CERTIFICADA POR:

Esta revista "no aplica" cargos por publicación en ninguna etapa del proceso editorial.
Dirección postal: Calle 51A y Avenida 5 de Septiembre Cienfuegos, Cuba Código postal: 55100.
http://www.revfinlay.sld.cu
Telefono: +53 43 516602. Telefax: +53 43 517733.
amgiraldoni@infomed.sld.cu
ISSN: 2221-2434
RNPS: 5129